Физико-химические методы исследования, 11 заданий
| Код | 225556 | ||
| Дата создания | 2016 | ||
| Страниц | 14 ( 14 шрифт, полуторный интервал ) | ||
|
Файлы
|
|||
|
Без ожидания: файлы доступны для скачивания сразу после оплаты.
Ручная проверка: файлы открываются и полностью соответствуют описанию.
|
|||
Образцы страниц развернуть (14)









Фрагмент работы для ознакомления
Задание 1
Через колонку, содержащую катионит в Н+- форме пропустили анализируемый раствор, содержащий ионы кадмия. Вытекающий раствор собрали в мерную колбу вместимостью 100 мл. На титрование 10 мл полученного раствора израсходовали 8,5 мл 0,0125 М раствора NaOH. Сколько граммов кадмия содержал исследуемый раствор?
Дано:
V(NaOH) = 8.5 см3
С (NaOH) = 0.0125 моль/〖дм〗^3
Vp-pa = 10 см3
Vколбы = 100 см3
Решение
...
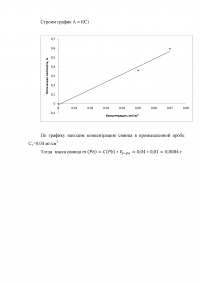
Задание 2
Для определения свинца в промышленном растворе 10 мл его поместили в мерную колбу вместимостью 100 мл и приготовили окрашенный раствор с сульфарсазеном. Оптическая плотность полученного раствора, измеренная относительно раствора сравнения, содержащего 0,002 г Pb в 100 мл, равна 0,23. Оптическая плотность стандартных растворов, содержащих в 100 мл 0,005 и 0,007 г Pb относительно того же раствора сравнения равна соответственно 0,360 и 0,595. Вычислите концентрацию Pb (г/л) в промышленном растворе.
Дано:
m1 (Pb)=0,005 г
m2 (Pb)=0,007 г
Vколбы=100 см3
А1=0,36
А2=0,595
Ах=0,23
Vp-pa=10 см3
Решение
...
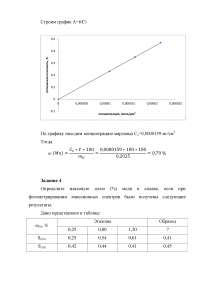
Задание 3
Для определения марганца навеску стали массой 0,2025 г растворили и получили 100 мл, содержащего ионы MnO4-. Оптическая плотность полученного раствора составила 0,32. Для построения градуировочного графика в мерные колбы на 100 мл поместили 10, 15, 20 мл стандартного раствора КМnO4 c TMn = 0,0001090 г/мл и разбавили до метки водой. Оптическая плотность составила 0,23; 0,35; 0,47. Определите массовую долю (%) Mn в стали.
Дано:
mн=0,2025 г
Vколбы=100 см3
А1=0,23
А2=0,35
А3=0,47
Ах=0,32
TMn = 0,0001090 г/см3
V1=10 см3
V2=15 см3
V3=20 см3
Решение
...
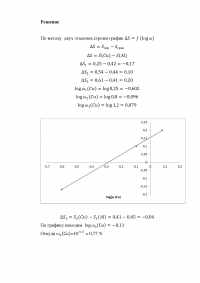
Задание 4
Определите массовую долю (%) меди в сплаве, если при фотометрировании эмиссионных спектров были получены следующие результаты:
Дано представлено в таблице:
| ωCu, % | Эталоны | Образец | ||
| 0,25 | 0,80 | 1,20 | ? | |
| S(Cu) | 0,25 | 0,54 | 0,61 | 0,41 |
| S(Al) | 0,42 | 0,44 | 0,41 | 0,45 |
Решение
...
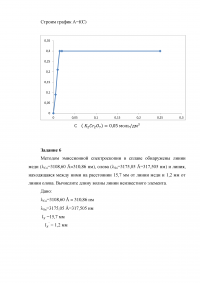
Задание 5
В электролите определяли содержание К2СrО4 методом турбидиметрического титрования 0,05Н раствором Рb(NO3)2. При титровании 10 мл электролита получили следующие данные:
| V (мл) | 1,0 | 2,0 | 3,0 | 4,0 | 5,0 | 6,0 |
| А | 0,09 | 0,21 | 0,30 | 0,30 | 0,30 | 0,30 |
Решение
...
Задание 6
Методом эмиссионной спектроскопии в сплаве обнаружены линии меди (Сu=3108,60 Å=310,86 нм), олова (Sn=3175,05 Å=317,505 нм) и линия, находящаяся между ними на расстоянии 15,7 мм от линии меди и 1,2 мм от линии олова. Вычислите длину волны линии неизвестного элемента.
Дано:
Сu=3108,60 Å = 310,86 нм
Sn=3175,05 Å=317,505 нм
l_x =15,7 мм
l`x = 1,2 мм
Решение
...
Задание 7
Из навески 2,0 г стали ванадий перевели в раствор и оттитровали 0,1н раствором сульфата железа (II)
Определите массовую долю ванадия в стали по следующим результатам потенциометрического титрования
Дано:
| VFeSO4, мл | 2,0 | 10,0 | 18,0 | 19,8 | 20,0 | 20,2 | 22,0 |
| Е, мВ | 1058 | 999 | 940 | 901 | 885 | 841 | 830 |
Решение
...
Задание 8
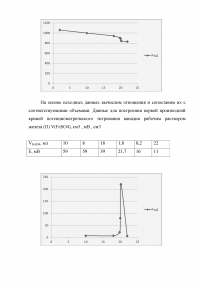
Для определения свинца в сточной воде пробу объемом 10 мл поместили в полярографическую ячейку, содержащую 5 м 1М гидроксида натрия. Величина предельного тока в квадратноволновом режиме полярографирования при
Е= –0,765В составила 35 мм диаграммной ленты. При добавлении в ячейку 2 мл 2×10-5М раствора нитрата свинца высота пика увеличилась до 75 мм. Определите массовую концентрацию свинца в воде.
Дано:
Vпробы=10 см3
V(NaOH) =5 см3
C(NaOH) = 1 моль/дм3
hx=35 мм
hx+s=75 мм
Решение
...
Задание 9
При определении свинца и цинка прокачали через фильтр 3000 л воздуха. Фильтр с пробой разложили в 10 мл смеси серной и азотной кислот. При полярографировании в режиме переменного тока высота пика цинка оказалась равной 48 мм, а высота пика свинца – 22 мм. При полярографировании стандартных растворов с С(Zn)=1×10-6моль/л и С(Рb) = 3×10-7 моль/л в том же фоне получили высоты пиков 34 и 42 мм соответственно. Определите содержание этих компонентов в 1 м3 воздуха.
Дано:
Vпробы= 3 м3
V(NaOH) =5 см3
C(NaOH) = 1 моль/дм3
hx (Zn) =34 мм
hx+s (Zn)=48 мм
hx (Pb) 22 мм
hx+s (Pb)=42 мм
С(Zn)=1×10-6моль/л
С(Рb) = 3×10-7 моль/л
Решение
...
Задание 10
Чему равна удельная электропроводность 0,001М раствора нитрата калия, если степень диссоциации равна 0,92, подвижности нитрат-ионов и ионов калия равны соответственно 71,5 и 75,3.
Дано:
C (KNO_3) =0,001 моль/дм3
λ_+^0 (К^+)=75,3
λ_-^0 (〖NO〗_3^-)=71,5
Α=0,92
Решение
...
Задание 11
При электролизе двухвалентного металла при силе тока 1А за 20 мин выделилось 0,4065 г металлического осадка. Что это за металл? Рассчитайте его электрохимический эквивалент.
Решение
...